AK SA TI ČLÁNOK BUDE PÁČIŤ NEVÁHAJ A PODPOR DETSKÚ ONKOLÓGIU DOBROVOĽNÝM PRÍSPEVKOM:
SVETIELKO NÁDEJE, o.z.
Detská fakultná nemocnica s poliklinikou
Nám. L. Svobodu 4
974 09 Banská Bystrica
www.svetielkonadeje.sk
IČO: 3788 9346
DIČ: 2021703200
Registrácia: Ministerstvo vnútra SR, č. spisu VVS/1- 900/90-16888 z 24.5.2002
Platobné údaje pre záujemcov o podporu našej činnosti:
IBAN: SK83 1100 0000 0026 2075 6262
Špecifický symbol: 45000

… ako molekula, ktorá určuje osud ľudstva
Lieberman a Long (2023) uvádzajú, že dopamín objavila v roku 1957 výskumníčka Kathleen Montaguová v nemocnici neďaleko Londýna. Na začiatku sa dopamín považoval za látku, ktorú telo používa pri produkcii epinefrínu (adrenalínu). Čoskoro si však vedci začali uvedomovať jeho význam. Dopamín produkuje len 0,0005 percenta mozgových buniek (päť z milióna), no tieto bunky majú obrovský vplyv na ľudské správanie. Keď sa dopamín uvoľnil v mozgu dobrovoľných účastníkov výskumu, zažívali pocity radosti a boli ochotní urobiť čokoľvek, aby aktivovali tieto cenné bunky.
Kde sa vlastne dopamín tvorí?
Podľa Čiháka (2016) je nucleus accumbens (NAcc), známy aj ako accumbens nucleus alebo nucleus accumbens septi, súčasťou bazálnych ganglií predného mozgu. Nachádza sa blízko laterálneho a zadného hypotalamu, v dorzálnej časti stredného mozgu a v mediálnej oblasti gyrus parahippocampalis pred čuchovou kôrou. Ide o párové jadrá, ktoré sú umiestnené v prednej časti nucleus caudatus a putamen, pričom sa odlišujú mikroskopickou anatomickou štruktúrou. NAcc je tvorený zhlukom neurónov v rámci prúžkovaného telesa (striata).
Podľa Bolekovej (2015) sa corpus striatum skladá z nucleus caudatus a nucleus lentiformis. Tieto dve hlavné hmoty jadier sú uložené vnútri mozgových hemisfér, medzi lôžkom a mozgovou kôrou (neocortex). Čihák (2016) ďalej uvádza, že NAcc sa morfologicky a funkčne skladá z dvoch oddielov: vnútornej drene a povrchového plášťa. Spojenia medzi nucleus accumbens a corpus amygdaloideum sú zodpovedné za niektoré pudy, najmä vznik závislostí. NAcc má tiež kľúčovú úlohu ako zhromažďovač endogénne syntetizovaného dopamínu, pričom zohráva dôležitú úlohu v mechanizmoch motivácie, odmeny, trestu, potešenia, smiechu, závislostí, strachu, agresie, spánku a prežívania zamilovanosti. Pri nadbytku dopamínu môže viesť k psychózam, zatiaľ čo jeho nedostatok je spojený s rozvojom Parkinsonovej choroby a tiež s placebo efektom.
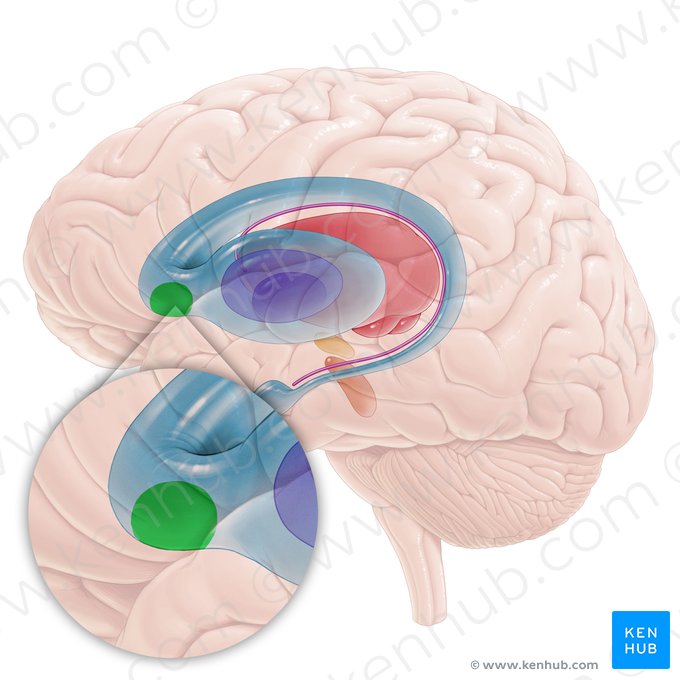
Obrázok 1 NAcc, Nucleus accumbens (Zdroj: Kenhub)
Podľa Mravca (2016) sú katecholamíny chemické látky obsahujúce katecholové jadro, medzi ktoré patrí dopamín, noradrenalín a adrenalín. Tieto látky fungujú ako neurotransmitery aj hormóny. Väčšina dopaminergných hormónov sa nachádza v dvoch blízkych oblastiach stredného mozgu: v substantia nigra, pars compacta a vo ventrálnej tegmentálnej oblasti (VTA). Dopamín sa syntetizuje z aminokyseliny tyrozínu, ktorá sa prevažne získava z cirkulácie pečene. Patologické poškodenie dopaminergických buniek v substantia nigra a následný nedostatok dopamínu v bazálnych gangliách sú spojené s Parkinsonovou chorobou. Predpokladá sa, že dysfunkcia dopaminergného systému zohráva úlohu v etiopatogenéze Huntingtonovej choroby, schizofrénie, depresie, Tourettovho syndrómu, závislosti na látkach, porúch príjmu potravy a poruchách pozornosti.
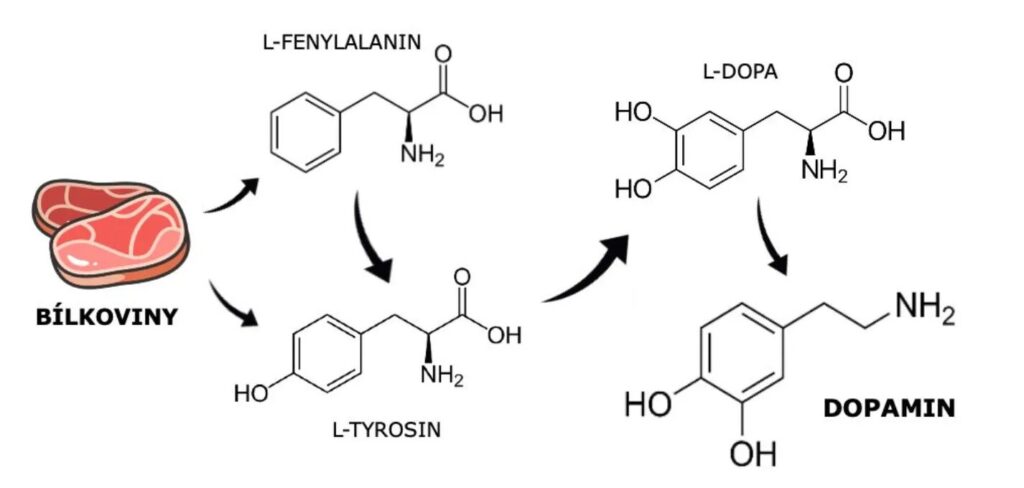
Obrázok 2 Syntéza dopamínu (Zdroj: https://aktin.sk/dopamin-aku-funkciu-ma-v-tele-a-preco-je-taky-dolezity)
Dopamín je kľúčový neurotransmiter, ktorý zohráva dôležitú úlohu v komplexných nervových obvodoch mozgu, ovplyvňujúc psychologické a fyziologické procesy. Jeho význam v odmeňovacom systéme je zásadný, pretože funguje ako silný motivátor, ktorý podnecuje jednotlivcov k pozitívnemu správaniu. Keď sa jednotlivci stretávajú s pozitívnymi podnetmi, dopaminergný systém riadi uvoľňovanie dopamínu, čím uľahčuje jeho prenos do rôznych oblastí mozgu. Podľa Javorku (2009) motivácia zahŕňa kombináciu vrodených a osvojených poznatkov, ktoré ovplyvňujú správanie jedinca v danom okamihu. Pohnútky k správaniu usmerňujú jedinca k uspokojeniu jeho základných potrieb, čím sa dosahuje ich oslabenie alebo zánik, napríklad prijatím potravy na zahánenie hladu.
Uspokojenie apetenčných potrieb alebo vyhýbanie sa nepríjemným situáciám sa nazýva odmena, zatiaľ čo vystavenie sa negatívnym podnetom sa považuje za trest. V zásade sa každý jedinec snaží o maximálne odmeňovanie a minimalizovanie trestov. Na základe stimulácie rôznych oblastí mozgu sa rozlišujú tri typy behaviorálnych odpovedí: indiferentné (asi 60 % mozgových štruktúr), odmietavé (okolo 5 %) a vysoko repetitívne (približne 35 %). Oblasti mozgu, ktorých stimulácia vedie k odmietavej odpovedi, tvoria systém trestu, ktorý sa nachádza najmä v laterálnom a zadnom hypotalame, v dorzálnej časti stredného mozgu a v mediálnej oblasti gyrus parahippocampalis.
Opakom je systém odmeny, pričom mnohé štúdie zdôrazňujú úlohu dopamínu ako prediktívneho neurotransmitera, ktorý je aktivovaný počas očakávania odmien. Táto aktivita vyvoláva radostné pocity, ktoré motivujú jednotlivcov k účasti na práci a vzdelávaní. U osôb závislých od drog sa však dopamín zúčastňuje anticipačných procesov, čo vedie k intenzívnejšej dopaminergnej reakcii a precitlivenosti na drogové stimuly. Pri užívaní drog dochádza k prudkému zvýšeniu dopamínu v mozgu, čo vyvoláva silné očakávanie a túžbu po drogách.
S dlhodobým užívaním drog sa vyvíja tolerancia v dôsledku nadmernej stimulácie dopamínových dráh, čo núti jednotlivcov zvyšovať dávky, aby dosiahli rovnakú úroveň uspokojenia. Týmto spôsobom sa vyvolávajú trvalé zmeny v dopamínových signálnych dráhach, čo môže viesť k anhedónii, stav, v ktorom jedinci nie sú schopní pociťovať potešenie z bežných odmien po vysadení drog. Tento jav vysvetľuje vysoké riziko recidívy u závislých aj po úspešnej detoxikácii.
Dopamín má významný vplyv na reguláciu emócií a emocionálnu pohodu. Pozitívne skúsenosti a vzrušenie stimulujú špecifické oblasti mozgu k uvoľneniu vyšších hladín dopamínu, čo vyvoláva kaskádu pozitívnych emócií. Látky ako heroín, kokaín a metamfetamín spôsobujú rýchly nárast hladiny dopamínu, prekračujúc jeho prirodzené fyziologické úrovne, čo vedie k intenzívnej rozkoši, ale rýchlo nasleduje pokles dopamínu a negatívne emócie.
V spánkovom cykle sa zúčastňuje niekoľko hormónov, vrátane serotonínu, ktorý pomáha regulovať pomalý a rýchly pohyb očí. Norepinefrín aktivuje epifýzu, čím stimuluje uvoľnenie melatonínu podľa cirkadiánneho rytmu. Norepinefrín spúšťa uvoľňovanie melatonínu viazaním sa na β1 a α1B adrenergné receptory, ktoré sú zodpovedné za produkciu melatonínu.
Serotonín, ktorý je prekurzorom melatonínu, hrá dôležitú úlohu v cykle spánku a bdenia. Zatiaľ čo serotonín a norepinefrín podporujú spánok, dopamín môže tento účinok zvrátiť. Dopamín pôsobí ako antagonista, ktorý znižuje produkciu a uvoľňovanie melatonínu. Dopaminergné neuróny vysielajú impulzy do kortikálnych a subkortikálnych oblastí, čím vytvárajú vzorce mozgovej a svalovej aktivity charakteristické pre bdenie a rýchly pohyb očí.
Dopamín môže vyvolať prebúdzanie a počas bdenia zvyšuje svalovú aktivitu. V tomto stave môže jednotlivec generovať nízke amplitúdy rýchlych oscilácií v gama aktivite, ktoré zvyšujú svalovú aktivitu. Niekedy môže dopamín viesť k poruchám spánku, ako je spánková paralýza, pri ktorej je svalová aktivita inhibovaná. Počas REM spánku vykazujú kôra a subkortikálna oblasť nízku amplitúdu rýchlych gama oscilačných frekvencií, podobne ako pri bdení, avšak svalová aktivita je inhibovaná rýchlym pohybom očí, ktorý je tiež spojený so zvýšenou hladinou dopamínu.
Čo je to dopaminergná osobnosť?
Lieberman a Long (2023) uvádzajú, že niektorí ľudia majú aktívnejšie dopaminergné obvody ako iní, pričom vedci identifikovali množstvo génov, ktoré prispievajú k rozvoju takýchto osobnostných typov. Zvýšená aktivita dopamínu sa môže prejaviť rôznymi spôsobmi; niektorí jedinci môžu byť impulzívni alebo majú problém nájsť potrebné uspokojenie. Naopak, jedinec s vysoko aktívnym riadiacim obvodom môže byť chladný, vypočítavý, bezohľadný a málo emocionálny.
Zaujímavá výskumná štúdia, korelát medzi kofeínom a hladinou dopamínu
Podľa výskumu môže konzumácia kávy dokonca pomôcť predchádzať Alzheimerovej chorobe alebo zabrániť intelektuálnemu poklesu tým, že znižuje množstvo škodlivých amyloidných plakov v mozgu. Experimenty naznačujú, že kofeín znižuje interakciu medzi beta-amyloidom. Týmto spôsobom môžeme usudzovať, že príjem kofeínu môže pôsobiť ako liek na Parkinsonovu a Alzheimerovu chorobu. Hlavným mechanizmom, prostredníctvom ktorého kofeín interaguje s Parkinsonovou chorobou, je inhibícia adenozínergného systému a prípadne modulácia dopaminergného systému. Kofeín je kľúčovou zložkou na vyvolanie zmien v správaní, pričom dve šálky kávy s kofeínom dokázali v závislosti od dávky zabrániť kataleptickému stavu vyvolanému haloperidolom. To naznačuje, že môže existovať pravdepodobný prístup k motorickej dysfunkcii spojené s Parkinsonovou chorobou.
Literatúra
ČIHÁK, R. (2016). Anatomie 3. Praha: Grada, 832 s. ISBN 978-8024-756-363.
HÖGLUND, E. – ØVERLI, Ø. –WINBERG, S. Tryptophan metabolic pathways and brain serotonergic activity: a comparative review. Frontiers in Endocrinology, 2019, 10:158. Dostupné z: https://www.frontiersin.org/articles/10.3389/fendo.2019.00158/full
JAVORKA, K. et al. (2009). Lekárska fyziológia. Martin: Osveta, 742 s. ISBN 978-80-8063-291-5.
LIEBERMAN, D. Z. – LONG, M. E. (2023). Dopamin. Praha: Dokořán a Argo, 301 s. ISBN 978-80-7675-135-4.
LOVÁSOVÁ, K. – KLUCHOVÁ, D. – BOLEKOVÁ, A. (2015). Neuroanatómia pre psychológov, štruktúry a funkcie nervového systému. Univerzita Pavla Jozefa Šafárika v Košiciach, Filozofická fakulta, 219 s. ISBN 978-80-8152-231-4.
PEČEŇÁK, J. – KOŘÍNKOVÁ, V. – BARTL, I. – HOLLÝ, M. – KRÁLOVÁ, M. – MRAVEC, B. – NAGY, M. – ONDIČOVÁ, K. – ONDREJKA, I. – TURČÁNI, P. – TURČEK, M. – VIŠŇOVSKÝ, E. (2016). Psychofarmakológia. Wolter Kluwer, s.r.o. 666 s. ISBN 978-80-8168-542-2.
PETER, M.C. The role of dopamine in sleep regulation. 2012, 42(6):287-9. Dostupné z: https://www.eurekalert.org/pub_releases/2012-06/plos-tro061412.ph
TAKATA, Y.–OISHI, Y. –ZHOU, X.Z.– HASEGAWA, E.–TAKAHASHI, K.– CHERASSE, Y.– SAKURAI, T., LAZARUS, M. Sleep and wakefulness are controlled by ventral medial midbrain/pons GABAergic neurons in mice. Journal of Neuroscience, 2018, 38(47):10080-92. Dostupné z: https://www.jneurosci.org/content/38/47/10080.full
VOLKOW, N.D.–TOMASI, D.–WANG, G.J.–TELANG, F.,F–OWLER, J.S.– LOGAN, J.–BENVENISTE, H.–KIM, R., THANOS, P.K., FERRÉ, S. Evidence that sleep deprivation down regulates dopamine D2R in ventral striatum in the human brain. Journal of Neuroscience, 2012, 32(19):6711-7. Dostupné z: https://www.jneurosci.org/content/32/19/6711.short
