AK SA TI ČLÁNOK BUDE PÁČIŤ NEVÁHAJ A PODPOR DETSKÚ ONKOLÓGIU DOBROVOĽNÝM PRÍSPEVKOM:
SVETIELKO NÁDEJE, o.z.
Detská fakultná nemocnica s poliklinikou
Nám. L. Svobodu 4
974 09 Banská Bystrica
www.svetielkonadeje.sk
IČO: 3788 9346
DIČ: 2021703200
Registrácia: Ministerstvo vnútra SR, č. spisu VVS/1- 900/90-16888 z 24.5.2002
Platobné údaje pre záujemcov o podporu našej činnosti:
IBAN: SK83 1100 0000 0026 2075 6262
Špecifický symbol: 45000

Anatomický versus chemický základ neurotransmisie
Čo je neurotransmisia?
Ako uvádza profesor Stahl (2013) neurotransmisia sa dá opísať mnohými spôsobmi: anatomicky, chemicky, elektricky. Anatomický základ neurotransmisie sú neuróny a spojenia medzi nimi, nazývané synapsie , niekedy tiež označované ako anatomicky adresovaný nervový systém, komplex „pevne zapojených“ synaptických spojení medzi neurónmi, podobne ako milióny telefónnych káblov v tisíckach káblových vedení. Anatomicky adresovaný mozog je teda komplexný schéma zapojenia, prenášajúca elektrické impulzy tam, kde je „kábel“ zapojený (t.j. na synapsií).
Synapsie
- Stahl (2013) spomína, že synapsie môžu vzniknúť na mnohých častiach neurónu, nielen na dendritoch ako axodendritické synapsie, ale aj na some ako axosomatické synapsie a dokonca na začiatku a na konci axónov (axoaxónové synapsie) .
- Takéto synapsie sú považované za „asymetrické“, pretože komunikácia je štrukturálne navrhnutá, aby bola jednosmerná; to znamená, anterográdne z axónu prvého neurónu na dendrit, somu alebo axón druhého neurónu
- To znamená, že existujú presynaptické prvky, ktoré sa líšia od postsynaptických prvkov.
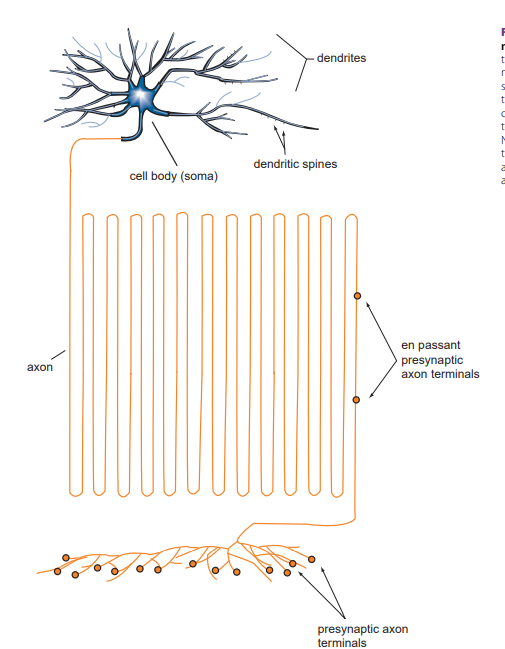
Obrázok 1 Všeobecná štruktúra neurónu (Zdroj: STAHL, S. M., 2013)
Neurotransmitery
- Konkrétne, neurotransmiter je zabalený v presynaptickej nervovej termináli ako munícia v nabitej zbrani a potom je „vystrelený“ na postsynaptický neurón, aby cielil na jeho receptory.
Neuróny
- Neuróny sú bunky chemickej komunikácie v mozgu. Ľudský mozog sa skladá z desiatok miliárd neurónov, pričom každý je prepojený s tisíckami iných neurónov. Tak má mozog trilióny špecializovaných spojení známych ako synapsie.
- Neuróny majú rôzne veľkosti, dĺžky a tvary, ktoré určujú ich funkcie. Lokalizácia v mozgu taktiež ovplyvňuje funkciu. Keď neuróny nefungujú správne, môžu sa objaviť behaviorálne symptómy. Keď lieky ovplyvnia funkciu neurónov, behaviorálne symptómy môžu byť zmiernené, zhoršené alebo vzniknúť nové (Stahl, 2013).
Všeobecná štruktúra neurónu
Podľa Stahla (2013) aj keď táto učebnica často zobrazuje neuróny s generickou štruktúrou, pravdou je, že mnohé neuróny majú jedinečné štruktúry v závislosti od toho, kde sa v mozgu nachádzajú a akú majú funkciu. Všetky neuróny majú telo známe ako soma a sú štrukturálne nastavené tak, aby prijímali informácie od iných neurónov prostredníctvom dendritov, niekedy cez spine na dendritoch a často prostredníctvom zložitých rozvetvených „stromov“ dendritov. Neuróny sú taktiež štrukturálne nastavené tak, aby posielali informácie iným neurónom prostredníctvom axónu, ktorý tvorí presynaptické terminály, keď axón prechádza (en passant alebo na konci axónu (presynaptické axónové terminály).
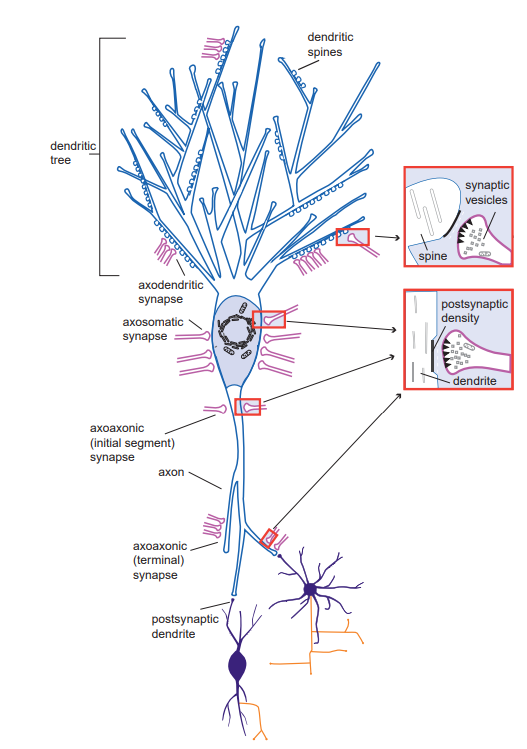
Obrázok 2 Axodendritické, axosomatické a axoaxonické spojenia (Zdroj: STAHL, S. M., 2013)
Neurotransmisia
Neurotransmisia má anatomickú infraštruktúru, ale v zásade je to veľmi elegantná chemická operácia. Doplnkom k anatomicky adresovanému nervovému systému je chemicky adresovaný nervový systém, ktorý tvorí chemický základ neurotransmisie: konkrétne, ako chemické signály (Stahla, 2013).
Proces neurotransmisie:
- Stahl (2013) tvrdí, že neurotransmitery sú kódované, dekódované, transdukované a posielané cez nervový systém.
- Pochopenie tohto procesu je nevyhnutné na porozumenie tomu, ako psychofarmakologické látky fungujú.
Cielenie liekov:
- Psychofarmakologické lieky cielia na špecifické chemické miesta, ktoré ovplyvňujú neurotransmisiu (Stahl, 2013).
Klinický význam:
- Podľa Stahla (2013) pevné porozumenie neurotransmisii je kľúčové pre klinikov.
- Znalosť mozgových obvodov, neurozobrazovania a genetiky môže zlepšiť klinickú prax.
- Toto porozumenie môže viesť k zlepšeniu diagnózy a liečby psychiatrických porúch.
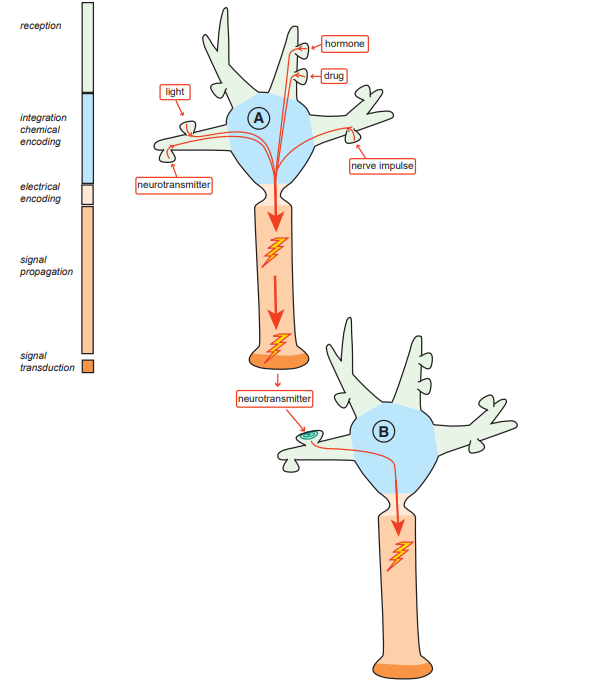
Obrázok 3 Klasická synaptická neurotransmisia (Zdroj: STAHL, S. M., 2013)
Oblasti mozgu a ich aplikácia na rôzne psychiatrické poruchy
Stahl (2013) spomína, že princípy chemickej neurotransmisie a to, ako sú aplikované na rôzne špecifické psychiatrické poruchy a liečené rôznymi špecifickými psychotropnými liekmi, sú diskutované v celej knihe.
Princípy chemickej neurotransmisie
Neurotransmitery
Existuje viac ako desiatky známych alebo podozrivých neurotransmiterov v mozgu. Pre psychofarmakológov je obzvlášť dôležité poznať šesť kľúčových neurotransmiterových systémov, na ktoré cielia psychotropné lieky:
- serotonín
- norepinefrín
- dopamín
- acetylcholín
- glutamát
- GABA (γ-aminomáselná kyselina)
Každý z nich je podrobne diskutovaný v klinických kapitolách súvisiacich so špecifickými liekmi, ktoré na ne cielia. Iné neurotransmitery, ktoré sú tiež dôležité neurotransmitery a neuromodulátory, ako histamín a rôzne neuropeptidy a hormóny. Niektoré neurotransmitery sú veľmi podobné liekom a nazývajú sa „Božia farmakopédia“. Napríklad je dobre známe, že mozog produkuje vlastný morfín (t.j. β-endorfín) a vlastnú marihuanu (t.j. anandamid). Mozog môže dokonca vyrábať vlastné antidepresíva, anxiolytiká a halucinogény. Lieky často napodobňujú prirodzené neurotransmitery mozgu a niektoré lieky boli objavené pred prirodzeným neurotransmiterom. Takže morfín bol používaný v klinickej praxi pred objavením β-endorfínu; marihuana sa fajčila pred objavením kanabinoidných receptorov a anandamidu; benzodiazepíny ako Valium (diazepam) a Xanax (alprazolam) (Stahl, 2013).
Neurotransmisia: klasická, retrográdna a objemová
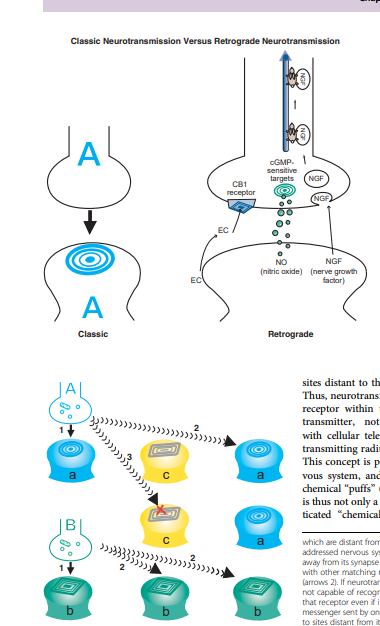
Obrázok 4 Retrográdna neurotransmisia (Zdroj: STAHL, S. M., 2013)
Stahl (2013) spomína, že klasická neurotransmisia začína elektrickým procesom, pri ktorom neuróny posielajú elektrické impulzy z jednej časti bunky do druhej časti tej istej bunky cez svoje axóny (pozri neurón A). Tieto elektrické impulzy však neskočia priamo na iné neuróny. Klasická neurotransmisia medzi neurónmi zahŕňa jeden neurón, ktorý vrhá chemického posla, alebo neurotransmiter, na receptory druhého neurónu (pozri synapsu medzi neurónom A a neurónom B na . To sa deje často, ale nie výlučne na miestach synaptických spojení. V ľudskom mozgu má sto miliárd neurónov, pričom každý vytvára tisíce synapsií s inými neurónmi, čo vedie k odhadovanému triliónu chemicky neurotransmitujúcich synapsií.
Komunikácia medzi všetkými týmito neurónmi na synapsiach je chemická, nie elektrická. To znamená, že elektrický impulz v prvom neuróne sa prevádza na chemický signál na synapse medzi ním a druhým neurónom v procese známej ako excitácia-sekrécia spájanie, prvá fáza chemickej neurotransmisie. To sa deje prevažne, ale nie výlučne v jednom smere, z presynaptického axonálneho terminálu na druhý postsynaptický neurón . Nakoniec neurotransmisia pokračuje v druhom neuróne buď tým, že sa chemická informácia z prvého neurónu opäť prevádza na elektrický impulz v druhom neuróne, alebo, možno elegantnejšie, tým, že chemická informácia z prvého neurónu spúšťa kaskádu ďalších chemických správ v druhom neuróne, aby zmenila molekulárne a genetické fungovanie tohto neurónu (Stahl, 2013).
Ako uvádza Stahl (2013) zaujímavým zvratom v chemickej neurotransmisii je objav, že postsynaptické neuróny môžu tiež „odpovedať“ svojim presynaptickým neurónom. Môžu to robiť prostredníctvom retrográdnej neurotransmisie z druhého neurónu na prvý na synapse medzi nimi . Chemikálie vyrobené špecificky ako retrográdne neurotransmitery na niektorých synapsiach zahŕňajú endokanabinoidy (EC, známe aj ako „endogénna marihuana“), ktoré sú syntetizované v postsynaptickom neuróne. Tieto sú potom uvoľnené a difúzujú k presynaptickým kanabinoidným receptorom, ako je receptor CB1, pravý panel). Ďalším retrográdnym neurotransmiterom je plynný neurotransmiter NO, alebo oxid dusnatý, ktorý je syntetizovaný postsynapticky a potom difúzuje von z postsynaptickej membrány do presynaptickej membrány, kde interaguje s cielenými miestami citlivými na cyklický guanozínmonofosfát (cGMP) . Tretia skupina retrográdnych neurotransmiterov sú neurotrofné faktory, ako NGF (faktor rastu nervov), ktorý je uvoľňovaný z postsynaptických miest a potom difúzuje k presynaptickému neurónu, kde je prijatý do vezikúl a transportovaný späť do jadra bunky prostredníctvom retrográdnych transportných systémov, aby interagoval s genomom tam. Čo tieto retrográdne neurotransmitery hovoria presynaptickému neurónu a ako to modifikuje alebo reguluje komunikáciu medzi presynaptickým a postsynaptickým neurónom, sú predmetom intenzívneho výskumu.
Okrem „obrátenej“ alebo retrográdnej neurotransmisie na synapsiach, niektoré neurotransmisie vôbec nepotrebujú synapsu! Neurotransmisia bez synapsy sa nazýva objemová neurotransmisia alebo nonsynaptická difúzna neurotransmisia (príklady sú uvedené na. Chemické posly, ktoré posiela jeden neurón druhému, môžu presakovať (Stahl, 2013).
Neurotransmisia a difúzia
Podľa Stahla (2013) neurotransmisia môže prebiehať na akomkoľvek kompatibilnom receptore v difúznej oblasti neurotransmitera, podobne ako moderná komunikácia s mobilnými telefónmi, ktoré fungujú v rámci prenosového dosahu danej mobilnej veže . Tento koncept je súčasťou chemicky adresovaného nervového systému, kde neurotransmisia prebieha v chemických „obláčikoch“ . Mozog teda nie je len zbierkou drôtov, ale aj sofistikovanou „chemickou polievkou“.
Chemická neurotransmisia a objemová neurotransmisia
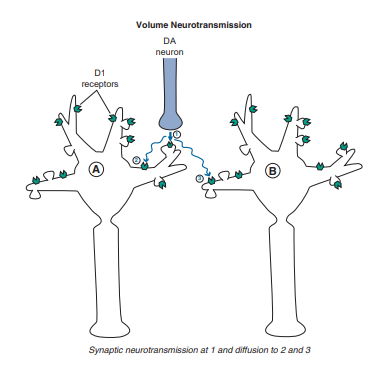
Obrázok 5 Objemová neurotransmisia: dopamín (Zdroj: STAHL, S. M. , 2013)
Stahl (2013) tvrdí, že chemicky adresovaný nervový systém je obzvlášť dôležitý pri zprostredkovaní účinkov liekov, ktoré pôsobia na rôzne receptory neurotransmiterov, pretože takéto lieky budú pôsobiť tam, kde sú relevantné receptory, a nie len tam, kde sú tieto receptory inervované synapsami anatomicky adresovaným nervovým systémom. Modifikácia objemovej neurotransmisie môže skutočne byť hlavným spôsobom, akým niektoré psychotropné lieky pôsobia v mozgu.
Dobrým príkladom objemovej neurotransmisie je pôsobenie dopamínu v prefrontálnej kôre. Tu je veľmi málo transportných čerpadiel na opätovné vstrebávanie dopamínu (dopamínové transportéry alebo DAT), ktoré ukončujú činnosť dopamínu uvoľneného v prefrontálnej kôre počas neurotransmisie. To je veľmi odlišné od iných oblastí mozgu, ako je striatum, kde sú čerpadlá na opätovné vstrebávanie dopamínu hojne prítomné. Takže, keď sa vyskytne dopamínová neurotransmisia na synapse v prefrontálnej kôre, dopamín má voľnosť pretekať z tejto synapsy a difúzovať k susedným dopamínovým receptorom, aby ich stimuloval, aj keď na týchto „pretekajúcich“ miestach nie je synapsa (Stahl, 2013).
Ako uvádza Stahl (2013) ďalším dôležitým príkladom objemovej neurotransmisie sú miesta autoreceptorov na monoamínových neurónoch (Obrázok 1-8). Na somatodendritickom konci neurónu sú autoreceptory, ktoré inhibujú uvoľňovanie neurotransmitera z axonálneho konca neurónu. Hoci niektoré opakujúce sa axonálne kolaterály a iné monoamínové neuróny môžu priamo inervovať somatodendritické receptory, tieto tzv. somatodendritické autoreceptory tiež prijímajú neurotransmiter z dendritického uvoľnenia. Tu nie je synapsa, len neurotransmiter, ktorý uniká z neurónu na jeho vlastné receptory. Povaha regulácie neurónu jeho somatodendritickými autoreceptormi je predmetom intenzívneho záujmu a teoreticky sa spája s mechanizmom účinku mnohých antidepresív. Hlavná myšlienka je, že nie všetka chemická neurotransmisia prebieha na synapsiách.
Excitácia-sekrécia
Stahl (2013) elektrický impulz v prvom – alebo presynaptickom – neuróne sa prevádza na chemický signál na synapse prostredníctvom procesu známeho ako excitácia-sekrécia. Akonáhle elektrický impulz prenikne do presynaptického axonálneho terminálu, spôsobí uvoľnenie chemického neurotransmitera, ktorý je tam uložený Elektrické impulzy otvárajú iónové kanály – ako napätím citlivé sodíkové kanály (VSSCs), tak aj napätím citlivé vápnikové kanály (VSCCs) – tým, že menia iónový náboj cez neurónové membrány. Keď sodík prúdi do presynaptického nervu cez sodíkové kanály v axónovej membráne, elektrický náboj akčného potenciálu sa pohybuje pozdĺž axónu, kým nedosiahne presynaptický nervový terminál, kde tiež otvára vápnikové kanály. Keď vápnik prúdi do presynaptického nervového terminálu, spôsobuje, že synaptické vezikuly pripevnené na vnútornej membráne vypustia svoj chemický obsah do synapsie. Cesta pre chemickú komunikáciu je teda pripravená predchádzajúcou syntézou neurotransmitera a jeho uložením v presynaptickom axonálnom termináli prvého neurónu.
Excitácia-sekrécia je teda spôsob, akým neurón prevádza elektrický podnet na chemickú udalosť. To sa deje veľmi rýchlo, akonáhle elektrický impulz vstúpi do presynaptického neurónu. Je tiež možné, aby neurón previedol chemickú správu z presynaptického neurónu späť na elektrickú chemickú správu v postsynaptickom neurónu otvorením iónových kanálov, ktoré sú tam prepojené s neurotransmitermi. To sa tiež deje veľmi rýchlo, keď chemické neurotransmitery otvárajú iónové kanály, ktoré menia tok náboja do neurónu a nakoniec vedú k akčným potenciálom v postsynaptickom neuróne. Takže proces neurotransmisie neustále prevádza chemické signály na elektrické signály a elektrické signály späť na chemické signály (Stahl, 2013).
Signálne transdukčné kaskády
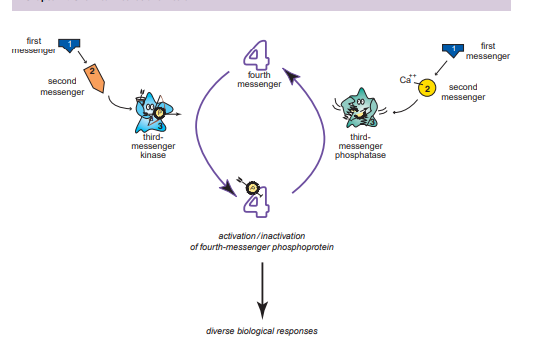
Obrázok 6 Kaskáda prenosu signálu (Zdroj: STAHL, S. M., 2013)
Prehľad
Stahl (2013) neurotransmisia môže byť chápaná ako súčasť oveľa väčšieho procesu než len komunikácia presynaptického axónu s postsynaptickým neurónom na synapse.
Signálne transdukčné kaskády
Podľa Stahla (2013) neurotransmisia môže byť chápaná ako komunikácia nielen medzi presynaptickým axónom a postsynaptickým neurónom na synapse, ale aj ako komunikácia z genómu presynaptického neurónu k genómu postsynaptického neurónu a potom späť z genómu postsynaptického neurónu k genómu presynaptického neurónu prostredníctvom retrográdnej neurotransmisie . Takýto proces zahŕňa dlhé reťazce chemických správ v oboch neurónoch, známych ako signálne transdukčné kaskády.
Signálne transdukčné kaskády vyvolané chemickou neurotransmisou teda zahŕňajú množstvo molekúl, počnúc neurotransmiterom ako prvým poslom, a pokračujúc druhými, tretími, štvrtými a ďalšími posolmi . Počiatočné udalosti sa odohrávajú za menej než sekundu, ale dlhodobé následky sú sprostredkované downstream posolmi, ktoré sa aktivujú za hodiny až dni, no môžu trvať mnoho dní alebo dokonca po celý život synapsie alebo neurónu. Signálne transdukčné kaskády sú do určitej miery podobné molekulárnemu „poštovému expresu“, kde špecializované molekuly pôsobia ako sekvencia jazdcov, ktorí odovzdávajú správu nasledujúcej špecializovanej molekule, až kým správa nedosiahne funkčné miesto, ako je expresia génov alebo aktivácia inak „spiacich“ a neaktívnych molekúl (Stahl , 2013).
Prehľad takéhoto molekulárneho „poštového expresu“, od prvého posla neurotransmitera cez niekoľko „molekulárnych jazdcov“ po produkciu rôznych biologických odpovedí, je znázornený na. Konkrétne, prvý posol neurotransmiter naľavo aktivuje produkciu chemického druhého posla, ktorý zase aktivuje tretieho posla, konkrétne enzým známy ako kináza, ktorý pridáva fosfátové skupiny na proteíny štvrtého posla, aby vytvoril fosfoproteíny . Ďalšia signálna transdukčná kaskáda je znázornená napravo, kde prvý posol neurotransmiter otvára iónový kanál, ktorý umožňuje vápniku vstúpiť do neurónu (Stahl, 2013).
Druhý posol a signálne transdukčné kaskády
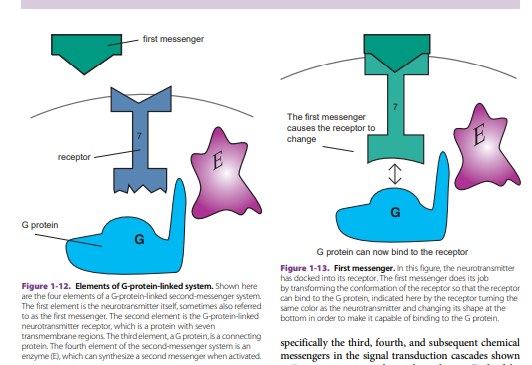
Obrázok 7, 8 Prvky systému prepojeného s G-proteínom, Prvý posol (Zdroj: STAHL, S. M., 2013)
Podľa Stahla (2013) v tejto kaskádovej sústave pôsobí vápnik ako druhý posol (Obrázok 1-9, napravo). Vápnik potom aktivuje iného tretieho posla, konkrétne enzým známy ako fosfatáza, ktorá odstraňuje fosfátové skupiny zo štvrtých poslov fosfoproteínov, čím sa tak vracajú účinky tretieho posla naľavo. Rovnováha medzi aktivitou kinázy a fosfatázy, signalizovaná rovnováhou medzi dvoma neurotransmitermi, ktoré aktivujú každý z nich, určuje stupeň chemickej aktivity downstream, ktorá sa prekladá na aktívne štvrté posly schopné vyvolať rôzne biologické odpovede, ako je expresia génov a synaptogenéza (Obrázok 1-9). Každé molekulárne miesto v transdukčnej kaskáde chemických a elektrických správ je potenciálnym miestom pre poruchu spojenú s duševnou chorobou; je to tiež potenciálny cieľ pre psychotropné lieky. Takže rôzne prvky viacerých signálnych transdukčných kaskád zohrávajú veľmi dôležité úlohy v psychofarmakológii.
Štyri z najdôležitejších signálnych transdukčných kaskád v mozgu sú zobrazené. Tieto zahŕňajú systémy prepojené s G-proteínmi, systémy prepojené s iónovými kanálmi, systémy prepojené s hormónmi a systémy prepojené s neurotrofínmi. Existuje mnoho chemických poslov pre každú z týchto štyroch kritických signálnych transdukčných kaskád; G-proteínové a iónovo-kanálové kaskády sú spúšťané neurotransmitermi. Mnohé z psychotropných liekov používaných v klinickej praxi dnes ciele jednu z týchto dvoch signálnych transdukčných kaskád. Lieky, ktoré cielia na systém prepojený s G-proteínmi, sú diskutované v kapitole 2; lieky, ktoré cielia na systém prepojený s iónovými kanálmi, sú diskutované v kapitole 3 (Stahla, 2013).
Tvorba druhého posla
Každá z štyroch signálnych transdukčných kaskád prenáša svoju správu z extracelulárneho prvého posla na intracelulárneho druhého posla. V prípade systémov prepojených s G-proteínmi je druhým poslom chemická látka, ale v prípade systému prepojeného s iónovými kanálmi môže byť druhým poslom ión, ako je vápnik. Pre niektoré systémy prepojené s hormónmi sa druhý posol vytvára, keď hormón nájde svoj receptor v cytoplazme a viaže sa naň, čím vytvorí komplex hormón–nukleárny receptor. Pre neurotrofíny existuje komplexná súprava rôznych druhých poslov, vrátane proteínov, ktoré sú kinázovými enzýmami so zložitými názvami. Transdukcia extracelulárneho prvého neurotransmitera z presynaptického neurónu na intracelulárneho druhého posla v postsynaptickom neuróne je podrobne známa pre niektoré druhé posly (Stahla, 2013).
Systémy druhého posla
Existujú štyri kľúčové prvky tohto systému druhého posla:
- Prvý posol neurotransmiter
- Receptor pre neurotransmiter, ktorý patrí do superrodiny receptorov, pričom všetky majú štruktúru siedmich transmembránových oblastí (označené číslom 7 na recepte v Obrázkoch 1-12 až 1-15).
- G-proteín, schopný viazať sa na určité konformácie receptoru neurotransmitera (7) a na enzýmový systém (E), ktorý môže syntetizovať druhý posol.
- Enzýmový systém samotný pre druhého posla.
Prvým krokom je viazanie neurotransmitera na jeho receptor. To mení konformáciu receptora, takže sa teraz môže prispôsobiť G-proteínu (Stahla, 2013).
Indikácie a prepojenia signálnych transdukčných kaskád
Podľa Stahla (2013) receptor sa zmení na zelenú a jeho tvar sa na spodnej strane zmení. Následne dochádza k viazaniu G-proteínu na túto novú konformáciu komplexu receptoru a neurotransmitera . Dva receptory spolupracujú: konkrétne receptor neurotransmitera a G-proteín, ktorý môžeme považovať za ďalší typ receptora spojeného s vnútornou membránou bunky. Táto spolupráca je znázornená , kde G-proteín zmení farbu na zelenú a jeho konformácia sa na pravej strane zmení, takže je teraz schopný viazať sa na enzým (E), ktorý syntetizuje druhého posla. Nakoniec sa enzým, v tomto prípade adenylátcykláza, viaže na G-proteín a syntetizuje cAMP (cyklický adenozínmonofosfát), ktorý slúži ako druhý posol . To je znázornené , kde sa enzým zmení na zelenú a generuje cAMP.
Nad druhým poslom k fosfoproteínovým poslom
Stahl (2013) spomína, že nedávny výskum začal objasňovať komplexné molekulárne prepojenia medzi druhým poslom a jeho konečnými účinkami na bunkové funkcie. Tieto prepojenia sú konkrétne tretí, štvrtý a nasledujúce chemické posly v signálnych transdukčných kaskádach znázornených. Každá zo štyroch tried signálnych transdukčných kaskád znázornených na Obrázku 1-11 nezačína iba s iným prvým poslom viažucim sa na unikátny receptor, ale vedie aj k aktivácii veľmi odlišných downstream druhých, tretích a nasledujúcich chemických poslov. Množstvo rôznych signálnych transdukčných kaskád umožňuje neurónom reagovať úžasne rôznorodo na celý rad chemických komunikačných systémov.
Aký je konečný cieľ signálnej transdukcie?
Existujú dva hlavné ciele signálnej transdukcie: fosfoproteíny a gény. Mnohé z intermediálnych cieľov na ceste k géne sú fosfoproteíny, ako sú štvrtí posli fosfoproteíny znázornené, ktoré ležia dormantne v neuróne, až kým ich signálna transdukcia nezobudí a nemôžu sa aktivovať.
Účinky znázornené na Obrázku 1-9 na štvrtých posloch fosfoproteínov ako cieľoch signálnej transdukcie môžeme vidieť podrobnejšie na Obrázkoch 1-16 až 1-19. Takže jedna signálna transdukčná dráha môže aktivovať tretieho posla kinázu prostredníctvom druhého posla cAMP (Obrázok 1-16), zatiaľ čo iná signálna transdukčná dráha môže aktivovať tretieho posla fosfatázu prostredníctvom druhého posla vápnika
Aktivácia kinázy a fosfatázy
V prípade aktivácie kinázy, dva kópie druhého posla cielené na každú regulačnú jednotku dormantného alebo „spiacého“ proteínovej kinázy (Obrázok 1-16). Keď sú niektoré proteínové kinázy neaktívne, existujú v diméroch (dve kópie enzýmu) a viažu sa na regulačnú jednotku, čím ich uvádzajú do konformácie, ktorá nie je aktívna. V tomto príklade, keď sa dve kópie cAMP viažu na každú regulačnú jednotku, regulačná jednotka sa oddelí od enzýmu, dimer sa rozpadne na dve kópie enzýmu a proteínová kináza je teraz aktivovaná, znázornená s lukom a šípom pripraveným na vystrelenie fosfátových skupín do nečakaných štvrtých poslov fosfoproteínov .
Medzitým sa formuje protivník proteínovej kinázy, konkrétne proteínová fosfatáza. Ďalší prvý posol otvára iónový kanál, čo umožňuje vstupe druhého posla vápniku, ktorý aktivuje fosfatázový enzým kalcineurín. V prítomnosti vápniku sa kalcineurín aktivuje, znázornený s prstami v tvare nožníc pripravenými na odstránenie fosfátových skupín zo štvrtých poslov fosfoproteínov .
Konflikt medzi kinázou a fosfatázou môžeme vidieť porovnaním toho, čo sa deje na Obrázkoch 1-18 a 1-19. Na Obrázku 1-18 tretí posol kináza pridáva fosfáty na rôzne štvrté posly fosfoproteíny, ako sú kanály viazané ligandom, kanály citlivé na napätie a enzýmy. Na Obrázku 1-19 tretí posol fosfatáza odstraňuje tieto fosfáty. Niekedy aktivácia fosforylácie aktivuje dormantný fosfoproteín; pre iné fosfoproteíny môže de-fosforylácia byť aktivujúca. Aktivácia štvrtých poslov fosfoproteínov môže zmeniť syntézu neurotransmiterov, ovplyvniť uvoľňovanie neurotransmiterov, zmeniť vodivosť iónov a vo všeobecnosti udržiavať aparát chemickej neurotransmisie
Rovnováha medzi fosforyláciou a de-fosforyláciou
Rovnováha medzi fosforyláciou a de-fosforyláciou štvrtých poslov kináz a fosfatáz zohráva kľúčovú úlohu v regulácii mnohých molekúl, ktoré sú kritické pre proces chemickej neurotransmisie.
Od druhého posla k fosfoproteínovej kaskáde, ktorá spúšťa expresiu génov
Konečná bunková funkcia, ktorú neurotransmisia často usiluje modifikovať, je expresia génov, či už zapínaním alebo vypínaním génu. Obe kaskády spúšťané neurotransmitermi pôsobia na systém CREB, ktorý reaguje na fosforyláciu svojich regulačných jednotiek. CREB je proteín viažuci sa na cAMP, transkripčný faktor v bunkovom jadre schopný aktivovať expresiu génov, najmä typu génov známych ako okamžité gény alebo gény okamžitej ranej fázy. Keď receptory prepojené s G-proteínmi aktivujú proteínovú kinázu A, tento aktivovaný enzým sa môže presunúť do bunkového jadra a pridať fosfátovú skupinu na CREB, čím sa aktivuje tento transkripčný faktor a spôsobí aktiváciu blízkeho génu. To vedie k expresii génov, najprv ako RNA a potom ako proteínu kódovaného génom.
Zaujímavé je, že receptorové kanály, ktoré zvyšujú intracelulárne hladiny druhého posla vápniku, môžu tiež aktivovať CREB jeho fosforyláciou. Proteín známy ako kalmodulín, ktorý interaguje s vápnikom, môže viesť k aktivácii určitých kináz nazývaných kinázy závislé od vápnika/kalmodulínu. Toto je úplne iný enzým než fosfatáza zobrazená na Obrázkoch 1-9, 1-17 a 1-19. Tu je aktivovaná kináza a nie fosfatáza. Keď je aktivovaná, táto kináza sa môže presunúť do
Aktivácia CREB a signálne transdukčné dráhy
Kináza sa môže presunúť do bunkového jadra a, rovnako ako kináza aktivovaná systémom G-proteínov, pridať fosfátovú skupinu na CREB a aktivovať tento transkripčný faktor, čím sa spúšťa expresia génov.
Dôležité je mať na pamäti, že vápnik dokáže aktivovať ako kinázy, tak aj fosfatázy. Existuje veľmi bohatá a niekedy mätúca škála kináz a fosfatáz, a konečný výsledok pôsobenia vápniku závisí od toho, ktoré substráty sú aktivované, pretože rôzne fosfatázy a kinázy cielia na veľmi odlišné substráty. Preto je dôležité mať na pamäti konkrétnu signálnu transdukčnú kaskádu, o ktorej sa diskutuje, a konkrétne fosfoproteíny pôsobiace ako posly v kaskáde, aby sme pochopili konečný efekt rôznych signálnych transdukčných kaskád.
Gény sú tiež konečným cieľom kaskády hormonálnej signálnej transdukcie. Niektoré hormóny, ako estrogén, tyroxín a kortizol, pôsobia na cytoplazmatické receptory, viažu sa na ne a vytvárajú komplex hormón–nukleárny receptor, ktorý sa presúva do bunkového jadra, nájde elementy v géne, ktoré môže ovplyvniť (nazývané hormonálne odpovedové elementy alebo HREs), a potom pôsobí ako transkripčný faktor na aktiváciu blízkych génov.
Nakoniec je aktivovaný veľmi zložitý systém signálnej transdukcie s hroznými názvami pre ich downstream posly signálnych kaskád, ktorý je aktivovaný neurotrofínmi a príbuznými molekulami. Aktivácia tohto systému prvými poslami neurotrofínmi vedie k aktivácii enzýmov, ktoré sú prevažne kinázami, pričom jedna kináza aktivuje ďalšiu, až nakoniec jedna z nich fosforyluje transkripčný faktor v bunkovom jadre a začína transkribovať gény . Ras je G-proteín, ktorý aktivuje kaskádu kináz s mätúcimi názvami. Pre tých, ktorí majú záujem o detaily, táto kaskáda začína aktiváciou Rafom, ktorý fosforyluje a aktivuje MEK (MAP kináza/ERK kináza, alebo mitogénom aktivovaná proteínová kináza/extracelulárne signály regulujúca kináza), čo aktivuje ERK
Aktivácia génov a signálne transdukčné dráhy
RKS (ribozomálna S6 kináza), MAPK (MAP kináza samotná) alebo GSK-3 (kináza glykogén syntázy), čo nakoniec vedie k zmenám v expresii génov. Mätúce? Nie je dôležité poznať názvy, ale pamätať si, že neurotrofíny spúšťajú dôležitú signálnu transdukčnú dráhu, ktorá aktivuje kinázové enzýmy jeden po druhom, čo nakoniec mení expresiu génov. Toto je dôležité vedieť, pretože táto signálna transdukčná dráha môže byť zodpovedná za expresiu génov, ktoré regulujú mnohé kritické funkcie neurónu, ako je synaptogenéza a prežitie buniek, ako aj plastické zmeny potrebné na učenie, pamäť a dokonca aj prejavy chorôb v rôznych mozgových obvodoch. Lieky a prostredie cielia na expresiu génov spôsobmi, ktoré sa práve začínajú rozumieť, vrátane toho, ako tieto akcie prispievajú k príčinám psychických chorôb a mechanizmom účinných liečebných postupov pre psychické choroby.
Medzitým je dôležité si uvedomiť, že veľmi široká škála génov je cielena všetkými štyrmi týmito signálnymi transdukčnými dráhami. Tieto sa pohybujú od génov, ktoré vytvárajú syntetické enzýmy pre neurotransmitery, po rastové faktory, proteíny cytoskeletu, proteíny bunkovej adhézie, iónové kanály, receptory a samotné intracelulárne signálne proteíny, medzi mnohými ďalšími. Keď sú gény exprimované akoukoľvek z signálnych transdukčných dráh znázornených na Obrázku 1-11, môže to viesť k vytvoreniu väčšieho alebo menšieho množstva akýchkoľvek z týchto proteínov. Syntéza takýchto proteínov je zjavne kritickým aspektom výkonu mnohých a rôznorodých funkcií neurónu. Rôzne biologické akcie sa uskutočňujú v neurónoch, ktoré menia správanie jednotlivcov v dôsledku expresie génov, ktorá je spúšťaná štyrmi hlavnými signálnymi transdukčnými kaskádami. Tieto funkcie zahŕňajú synaptogenézu, zosilnenie synapsie, neurogenézu, apoptózu, zvyšovanie alebo znižovanie efektivity spracovania informácií v kortikálnych obvodoch, ako aj správanie ako učenie, pamäť, antidepresívne reakcie na podávanie antidepresív, zníženie symptómov psychoterapiou a dokonca aj produkciu psychickej choroby.
Ako neurotransmisia spúšťa expresiu génov
Ako gén vyjadruje proteín, ktorý kóduje? Diskusia vyššie ukázala, ako molekulárny „poštový expres“ signálnej transdukcie má správu zakódovanú chemickou informáciou z komplexu neurotransmiter–receptor, ktorá sa prenáša od molekulárneho jazdca k molekulárnemu jazdcovi, až kým sa správa nedoručí do príslušnej fosfoproteínovej schránky alebo do schránky DNA v genóme postsynaptického neurónu Keďže najvýznamnejší spôsob, ako neurón zmeniť svoju funkciu, je zmeniť, ktoré gény sú zapnuté alebo vypnuté, je dôležité pochopiť molekulárne mechanizmy, ktorými neurotransmisia reguluje expresiu génov.
Koľko potenciálnych génov môže neurotransmisia cieliť? Odhaduje sa, že ľudský genóm obsahuje približne 20 000 až 30 000 génov umiestnených v 3 miliónoch bázových párov DNA na 23 chromozómoch. Neuveriteľné však je, že gény zaberajú len niekoľko percent tejto DNA. Ostatných 97 % sa kedysi považovalo za „odpad“ DNA, pretože nekóduje proteíny, ale teraz sa vie, že tieto sekcie DNA sú kritické na reguláciu toho, či je gén exprimovaný alebo tichý. Nie je dôležité len to, koľko génov máme, ale aj to, či, kedy, ako často a za akých okolností sú exprimované, čo sa zdá byť dôležitým faktorom pri regulácii funkcie neurónu. Tieto isté faktory expresie génov sú teraz považované za základné aj pre účinky psychofarmakologických liekov a mechanizmy psychických porúch v centrálnom nervovom systéme.
Molekulárny mechanizmus expresie génov
Stahl (2013) uvádza, že chemická neurotransmisia prevádza obsadenosť receptoru neurotransmiterom na vytvorenie tretích, štvrtých a nasledujúcich poslov, ktorí nakoniec aktivujú transkripčné faktory, ktoré zapínajú gény Väčšina génov má dve oblasti: kódujúcu oblasť a regulačnú oblasť s enhancerami a promotormi transkripcie génov. Kódujúca oblasť je priamym vzorcom na výrobu svojej zodpovedajúcej RNA. Táto DNA môže byť transkribovaná do svojej RNA s pomocou enzýmu nazývaného RNA polymeráza. Avšak RNA polymeráza musí byť aktivovaná, inak nebude fungovať. Našťastie regulačná oblasť génu to môže spôsobiť. Má element enhancer a element promótor, ktoré môžu iniciovať expresiu génu s pomocou transkripčných faktorov. Transkripčné faktory sa môžu aktivovať, keď sú fosforylované, čo im umožňuje viazať sa na regulačnú oblasť génu . To následne aktivuje RNA polymerázu a začína sa transkripcia kódujúcej časti génu je do jeho mRNA.
Aktivácia génov pomocou Jun a Fos
Takže Jun a Fos slúžia na „prebudenie“ oveľa väčšej armády neaktívnych génov. Ktoré jednotlivé „následné“ gény sú povolané do aktívnej služby závisí od niekoľkých faktorov, pričom medzi nimi je aj to, ktorý neurotransmiter posiela správu, ako často ju posiela a či pracuje v súlade alebo v opozícii s inými neurotransmitermi, ktoré komunikujú s inými časťami toho istého neurónu súčasne. Keď sa Jun a Fos spoja, aby vytvorili transkripčný faktor typu leucínového zipsu, môže to viesť k aktivácii génov na výrobu čohokoľvek, čo si dokážete predstaviť, od enzýmov po receptory a štrukturálne proteíny (Stahl, 2013).
Zhrnutie procesu transkripcie génov
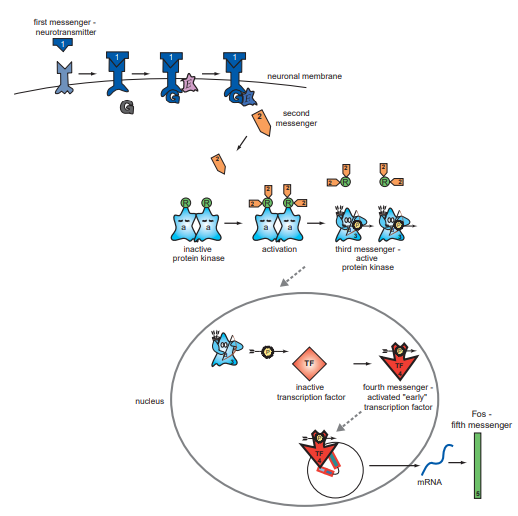
Obrázok 9 Regulácia génov neurotransmitermi (Zdroj: STAHL, S. M., 2013)
Stahl (2013) spomína, že môžeme sledovať udalosti od neurotransmitujúceho prvého posla až po transkripciu génov Keď je druhý posol cAMP vytvorený z jeho prvého posla neurotransmitera , môže interagovať s proteínovou kinázou ako tretím poslom. cAMP sa viaže na neaktívnu alebo spiacu verziu tohto enzýmu, „prebudí“ ho a aktivuje proteínovú kinázu. Akonáhle je prebudená, úlohou tretej poslovej proteínovej kinázy je aktivovať transkripčné faktory ich fosforyláciou. Robí to tak, že sa priamo presúva do bunkového jadra a nájde spiaci transkripčný faktor. Pridaním fosfátovej skupiny na transkripčný faktor dokáže proteínová kináza „prebudiť“ tento transkripčný faktor a vytvoriť štvrtého posla . Akonáhle je transkripčný faktor prebudený, viaže sa na gény a spôsobuje syntézu proteínov.
Syntéza génových produktov
Syntéza; v tomto prípade produkt okamžitého rannej fázy génu, ktorý funguje ako piaty posol. Dva takéto génové produkty sa spoja, aby vytvorili ďalší aktivovaný transkripčný faktor, a to je šiesty posol. Nakoniec šiesty posol spôsobuje expresiu produktu neskorého génu, ktorý by sa mohol považovať za produkt proteínu siedmeho posla aktivovaného génu. Tento produkt neskorého génu potom sprostredkuje biologickú reakciu dôležitú pre fungovanie neurónu. Samozrejme, molekulárne kaskády indukované neurotransmiterom vedú do bunkového jadra k zmenám nielen v syntéze vlastných receptorov, ale aj v syntéze mnohých ďalších dôležitých postsynaptických proteínov, vrátane enzýmov a receptorov pre iné neurotransmitery. Ak takéto zmeny v genetickej expresii vedú k zmenám (Stahl, 2013).
Vplyv génov na správanie
Podľa Stahla (2013) ak zmeny v spojeniach a funkciách, ktoré tieto spojenia vykonávajú, vedú k zmenám, je ľahké pochopiť, ako môžu gény modifikovať správanie. Detaily fungovania nervov — a teda správanie vyplývajúce z tohto nervového fungovania — sú kontrolované génmi a produktmi, ktoré produkujú. Keďže mentálne procesy a správanie, ktoré spôsobujú, pochádzajú zo spojení medzi neurónmi v mozgu, gény majú teda významnú kontrolu nad správaním.
Ale môže správanie modifikovať gény? Učenie, ako aj skúsenosti z prostredia môžu skutočne zmeniť, ktoré gény sú exprimované, a tak môžu viesť k zmenám v neurónových spojeniach. Týmto spôsobom môžu ľudské skúsenosti, vzdelávanie a dokonca aj psychoterapia zmeniť expresiu génov, ktoré menia rozloženie a „silnosť“ konkrétnych synaptických spojení. To môže viesť k dlhodobým zmenám v správaní spôsobeným pôvodnou skúsenosťou a sprostredkovaným genetickými zmenami vyvolanými touto pôvodnou skúsenosťou (Stahl, 2013).
Vzájomný vplyv génov a správania
Ako uvádza Stahl (2013) teda gény modifikujú správanie a správanie modifikuje gény. Gény priamo neregujú fungovanie neurónov. Namiesto toho priamo regulujú proteíny, ktoré vytvárajú fungovanie neurónov. Zmeny vo fungovaní musia počkať, kým sa uskutočnia zmeny v syntéze proteínov a kým sa začnú diať udalosti, ktoré spôsobujú.
Genetika a epigenetika v neurónovej funkcii
Genetika je DNA kód pre to, čo môže bunka transkribovať do špecifických typov RNA alebo prekladať do špecifických proteínov. Avšak, len preto, že v ľudskom genóme je viac ako 20 000 génov, neznamená to, že každý gén je exprimovaný, ani v mozgu. Epigenetika je paralelný systém, ktorý určuje, či je daný gén skutočne premenený na svoju špecifickú RNA a proteín, alebo či je ignorovaný alebo umlčaný. Ak je genóm lexikónom všetkých proteínových „slov“, potom je epigenóm „príbehom“, ktorý vzniká usporiadaním „slov“ do koherentného rozprávania. Genomický lexikón všetkých potenciálnych proteínov je rovnaký vo všetkých viac ako 10 miliardách neurónov v mozgu a v skutočnosti je rovnaký vo všetkých viac ako 200 typoch buniek v tele. Takže dej toho, ako sa normálny neurón stáva nefunkčným neurónom v psychickej poruche, ako aj to, ako sa neurón stáva neurónom namiesto pečeňovej bunky, závisí od výberu, ktoré konkrétne gény sú exprimované alebo umlčané. Okrem toho sú nefunkčné neuróny ovplyvnené dedičnými génmi, ktoré majú abnormálne nukleotidové sekvencie, ktoré, ak sú exprimované, prispievajú k duševným poruchám. Takže príbeh mozgu závisí nielen od toho, ktoré gény sú zdedené, ale aj od toho, či sú exprimované akékoľvek abnormálne gény, alebo dokonca či sú exprimované normálne gény, keď by mali byť tiché, alebo umlčané, keď by mali byť exprimované. Neurotransmisia, samotné gény, lieky a prostredie všetky regulujú, ktoré gény sú exprimované alebo umlčané, a teda všetky ovplyvňujú, či je príbeh mozgu presvedčivým naratívom, ako je učenie a pamäť, ľutovanou tragédiou, ako je zneužívanie drog, stresové reakcie a psychické poruchy, alebo terapeutickým zlepšením psychickej poruchy prostredníctvom liekov alebo psychoterapie (Stahl, 2013).
Aké sú molekulárne mechanizmy epigenetiky?
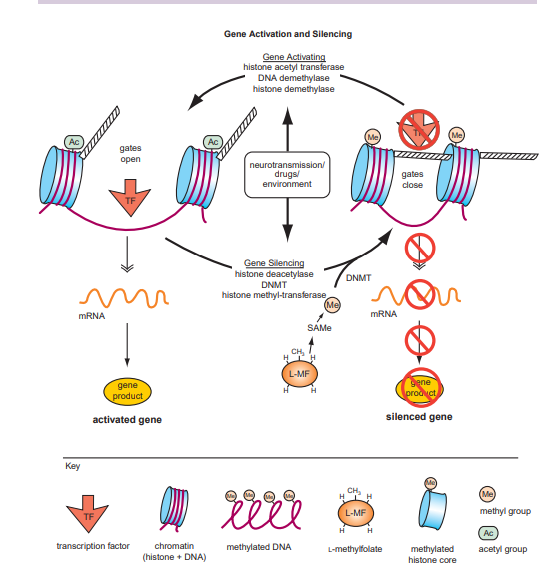
Obrázok 10 Aktivácia a zánik génov (Zdroj: STAHL, S. M., 2013)
Podľa Stahla (2013) epigenetické mechanizmy zapínajú a vypínajú gény modifikovaním štruktúry chromatínu v bunkovom jadre . Charakter bunky je zásadne určený jej chromatínom, látkou zloženou z nukleozómov. Nukleozómy sú oktet proteínov nazývaných históny, okolo ktorých je zabalená DNA . Epigenetická kontrola nad tým, či je gén čítaný (t. j. exprimovaný) alebo nie je čítaný (t. j. umlčaný), sa dosahuje modifikovaním štruktúry chromatínu. Chemické modifikácie, ktoré to môžu dosiahnuť, zahŕňajú nielen metyláciu, ale aj acetyláciu, fosforyláciu a iné procesy, ktoré sú regulované neurotransmisou, liekmi a prostredím. Napríklad, keď je DNA alebo históny metylované, kompaktizuje to chromatín a uzatvára prístup molekulárnym transkripčným faktorom k promótorovým oblastiam DNA, čo má za následok, že gén v tejto oblasti je umlčaný a nie je exprimovaný, takže sa nevyrába RNA ani proteín . Umlčaná DNA znamená molekulárne črty, ktoré nie sú súčasťou osobnosti danej bunky. Históny sú metylované enzýmami nazývanými histónové metyltransferázy, a toto je zvrátené enzýmami nazývanými histónové demetylázy . Metylácia histónov môže umlčať gény, zatiaľ čo demetylácia histónov môže aktivovať gény. DNA môže byť tiež metylovaná, a to tiež umlčuje gény. Demetylácia DNA toto zvracia. Metylácia DNA je regulovaná enzýmami nazývanými DNA metyltransferázy (DNMT), a demetylácia DNA enzýmami nazývanými DNA demetylázy . Existuje mnoho foriem metyltransferáz, a všetky označujú svoje substráty metylovými skupinami darovanými z l-metylfolátu prostredníctvom S-adenozylmetionínu (SAMe). Keď neurotransmisia, lieky alebo prostredie ovplyvňujú metyláciu, reguluje to, či sú gény epigeneticky umlčané alebo exprimované. Metylácia DNA môže nakoniec viesť aj k deacetylácii histónov, aktivovaním enzýmov nazývaných histónové deacetylázy (HDACs). Deacetylácia histónov má tiež umlčujúci účinok na expresiu géno. Metylácia a deacetylácia komprimujú chromatín, akoby sa uzavrela molekulárna brána. To zabraňuje prístupu transkripčných faktorov k promótorovým oblastiam, ktoré aktivujú gény; tým pádom sú gény umlčané a nie sú transkribované do RNA ani prekladané do proteínov . Na druhej strane, demetylácia a acetylácia robia presný opak: dekomprimujú chromatín, akoby sa otvorila molekulárna brána, a tým pádom môžu transkripčné faktory pristupovať k promótorovým oblastiam génov a aktivovať ich. Aktivované gény sa tak stávajú súčasťou molekulárnej osobnosti danej bunky (Stahl, 2013).
Ako epigenetika udržiava alebo mení status quo
Podľa Stahla (2013) niektoré enzýmy sa snažia udržiavať status quo bunky, ako napríklad DNMT1 (DNA metyltransferáza 1), ktorá udržiava metyláciu špecifických oblastí DNA a udržuje rôzne gény tiché po celý život. To znamená, že tento proces udržuje neurón neurónom a pečeňovú bunku pečeňovou bunkou, vrátane situácie, keď sa bunka delí na ďalšiu. Predpokladá sa, že metylácia sa udržuje na génoch, ktoré jedna bunka nepotrebuje, aj keď iný typ bunky by ich mohol potrebovať.
Predtým sa myslelo, že keď sa bunka diferencuje, epigenetický vzor aktivácie a umlčania génov zostáva stabilný po celý život tejto bunky. Teraz je však známe, že existujú rôzne okolnosti, za ktorých sa epigenetika môže zmeniť v zrelých, diferencovaných neurónoch. Hoci počiatočný epigenetický vzor neurónu je skutočne nastavený počas neurovývoja, aby každému neurónu dal jeho vlastnú celoživotnú „osobnosť“, teraz sa zdá, že príbeh niektorých neurónov reaguje na ich naratívne skúsenosti počas života so zmenou charakteru, čo vedie k de novo zmenám v ich epigenóme. V závislosti od toho, čo sa stane neurónu (ako je zneužívanie detí, stres v dospelosti, diétne nedostatky, produktívne nové stretnutia, psychoterapia, drogy a psychotropné terapeutické lieky), sa zdá, že predtým umlčané gény môžu byť aktivované a/alebo predtým aktívne gény môžu byť umlčané. Keď sa to stane, môžu sa vyskytnúť ako priaznivé, tak nepriaznivé vývojové zmeny v charaktere neurónov. Priaznivé epigenetické mechanizmy môžu byť aktivované, aby sa človek mohol učiť (napr. formovanie priestorovej pamäte) alebo zažiť terapeutické účinky psychofarmakologických činidiel. Na druhej strane nepriaznivé epigenetické mechanizmy môžu byť aktivované, aby sa človek stal závislým na drogách alebo zažil rôzne formy „abnormálneho učenia“, ako keď sa vyvinie podmienenie strachom, úzkostná porucha alebo chronická bolesť (Stahl, 2013).
Ako uvádza Stahl (2013) sa tieto epigenetické mechanizmy dostanú na miesto činu, zostáva presvedčivou neurobiologickou a psychiatrickou záhadou. Napriek tomu armáda vedeckých detektívov pracuje na týchto prípadoch a začína ukazovať, ako sú epigenetické mechanizmy mediátormi psychických porúch. Existuje tiež možnosť, že epigenetické mechanizmy môžu byť využité na liečbu závislostí, elimináciu strachu a prevenciu vzniku chronických bolestí. Môže byť dokonca možné zabrániť progresii chorôb psychických porúch, ako je schizofrénia, identifikovaním jednotlivcov s vysokým rizikom predtým, ako sa „zápletka zahustí“ a porucha sa neodvratne ustáli a neúprosne kráča k neželanému osudu.
Jedným z mechanizmov na zmenu status quo epigenomických vzorov v zrelej bunke je prostredníctvom de novo metylácie DNA typom enzýmu DNMT, známeho ako DNMT2 alebo DNMT3 . Tieto enzýmy cielia na neurónové gény na umlčanie, ktoré boli predtým aktívne v zrelom neuróne. Samozrejme, deacetylácia histónov v blízkosti predtým aktívnych génov by urobila to isté, t.j. umlčala by ich, a to je sprostredkované enzýmami nazývanými histónové deacetylázy (HDACs). Naopak, demetylácia alebo acetylácia aktivujú gény, ktoré boli predtým tiché. Skutočná otázka znie: ako neurón vie, ktoré gény zo svojich tisícov umlčať alebo aktivovať v reakcii na prostredie, vrátane stresu, drog a stravy? Ako sa to môže pokaziť, keď sa vyvinie psychická porucha? Táto časť príbehu zostáva zložitou záhadou, ale už bolo vykonaných niekoľko veľmi zaujímavých detektívnych prác rôznymi výskumníkmi, ktorí dúfajú, že pochopia, ako niektoré neurónové príbehy vyústi do psychiatrických tragédií. Tieto vyšetrovania môžu pripraviť pôdu na prepísanie naratívu rôznych psychických porúch terapeutickým zmenením epigenetiky kľúčových neurónových postáv, aby príbeh mal šťastný koniec (Stahl, 2013).
Literatúra
STAHL, S. M. (2013). Stahl’s Essential Psychopharmacology: Neuroscientific Basis and Practical Applications. 4. vyd. Cambridge: Cambridge University Press.
